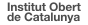Bateries i acumuladors
Com què la generació d’energia d’un camp fotovoltaic és variable i depèn de la radiació solar, aquesta no sempre està disponible. Per tant, en algunes instal·lacions s’emmagatzema l’energia, en bateries o acumuladors, en les hores de màxima generació, per tal d’utilitzar-la en les hores que no hi ha producció d’energia solar o en el moment de més demanda energètica de la instal·lació receptora.
Tipus de bateries
Una bateria és un conjunt d’acumuladors elèctrics connectats en sèrie o en paral·lel, amb una combinació concreta per donar uns valors determinats de tensió i de capacitat, que serveix per emmagatzemar electricitat.
Capacitat d'una bateria
La capacitat és la quantitat d’energia elèctrica que pot emmagatzemar una bateria.
Funcions d'una bateria
L’objectiu principal de les bateries depèn del tipus d’instal·lació:
Una bateria emmagatzema energia elèctrica.
Instal·lacions fotovoltaiques autònomes
En les instal·lacions fotovoltaiques autònomes, cal emmagatzemar l’energia captada durant les hores de radiació solar a fi de poder cobrir el subministrament durant les hores que no n’hi ha (cicle diari i cicle estacional).
- Les instal·lacions fotovoltaiques autònomes requereixen sistemes d’acumulació d’energia que:
- Subministraran energia en absència de radiació: nits i dies amb núvols, cicle diari…
- Mantindran estable el voltatge la instal·lació: la tensió a la sortida de les plaques varia en funció de la radiació incident i la càrrega connectada, per la qual cosa la connexió directa a plaques no és massa viable en la major part de les ocasions.
- Subministraran una potència instantània, durant un temps limitat, superior a la que el camp de plaques podria generar encara en el millor dels casos. És el cas de l’engegada de motors, com per exemple pot ser el motor d’una nevera.
- En les instal·lacions d’autoconsum les bateries emmagatzemen l’energia elèctrica que generen els panells solars que no es consumeix, de manera que s’evita que l’excedent se subministri a la xarxa de distribució elèctrica. Això permet utilitzar l’energia emmagatzemada quan el camp fotovoltaic no genera energia.
Principi de funcionament d'una bateria
La figura representa el principi de funcionament d’una bateria:
- Procés de descàrrega. Una bateria transforma l’energia química emmagatzemada en energia elèctrica, que subministra a la instal·lació quan cal alimentar dispositius elèctrics.
- Procés de càrrega. El procés de descàrrega és reversible, de manera que la bateria es pot recarregar quan s’alimenta amb un corrent elèctric, convertint l’energia elèctrica subministrada en energia química.
El tipus de bateria que tradicionalment s’ha utilitzat en les instal·lacions solars fotovoltaiques són el tipus plom àcid.
Aplicacions de les bateries
En funció de l’aplicació, les bateries es classifiquen de la manera següent:
- Bateries d’arrencada. S’utilitzen en automoció i estan dissenyades per subministrar intensitats de corrent elevat durant períodes de temps curts. Admeten cicles de descàrrega poc profunds.
- Bateries de tracció (figura). Estan pensades per a moure vehicles i carretons elèctrics. Són més econòmiques que les estacionàries i poden donar un bon servei en instal·lacions fotovoltaiques, sempre que es tingui en compte que requereixen un manteniment més freqüent.
- Bateries estacionàries. Estan dissenyades per treballar en règims de càrrega i descàrrega lents. S’utilitzen en les instal·lacions solars fotovoltaiques i en els sistemes d’alimentació ininterrompuda (SAI).
Les bateries que s’utilitzen en les instal·lacions solars fotovoltaiques són bateries estacionàries dissenyades per treballar en règims de càrrega i descàrrega lents.
Bateries de plom àcid
Les bateries que tradicionalment s’han utilitzat en les instal·lacions solars fotovoltaiques són les bateries de plom àcid.
-

- Bateria de plom àcid.
Una bateria transforma l’energia elèctrica que rep en energia química a partir de la reacció que es produeix quan dos materials diferents, com els elèctrodes de les plaques positiva i negativa d’una bateria, se submergeixen en un electròlit.
Electròlit
L’electròlit és una substància que, fosa o dissolta en un solvent ionitzant, es dissocia donant ions i, llavors, esdevé conductora de l’electricitat.
Al conjunt format per una parella d’elèctrodes (ànode o positiu i càtode o negatiu) en bany electrolític se l’anomena cel·la o vas de bateria.
En cada cel·la o element d’una bateria de plom àcid, l’electròlit està format per una solució d’àcid sulfúric (H2SO4) i aigua (H2O). La placa positiva de cada element està formada de diòxid de plom (PbO2) i la placa negativa de plom (Pb).
Tensió d'una cel·la
En una bateria de plom àcid convencional, la tensió és d’aproximadament 2 volts per cel·la. Per tant, per aconseguir bateries de més tensió cal associar diferents cel·les en sèrie fins a aconseguir la tensió desitjada.
Principi bàsic de funcionament de la bateria de plom àcid
Quan un acumulador de plom-àcid rep corrent elèctric, el sulfat de plom adherit a les plaques es transforma en plom que continua en les plaques i en àcid sulfúric que passa a l’electròlit, tal com reflecteix la següent fórmula de procés.

En el moment de la descàrrega el procés s’inverteix; per tant, l’àcid sulfúric es combina amb el plom de les plaques fins a formar sulfat de plom.

Estat de càrrega d'una bateria de Pb àcid en funció de la densitat de l'electròlit
La densitat de l’electròlit d’una bateria depèn de l’estat de càrrega, tal com es mostra a la figura. Quan la bateria es troba completament carregada, l’àcid sulfúric que conté l’electròlit és més gran que quan es troba descarregada, per tant, la seva densitat també ho és.
Si després de carregar una bateria, la densitat de l’electròlit no es correspon amb la que considerem normal en una bateria de Pb àcid, cal esperar que part de l’aigua s’hagi evaporat. Per tant, caldrà afegir aigua destil·lada, procés que forma part del manteniment d’aquest tipus de bateria.
Una densitat d’1,00 g/ml es correspon amb la densitat de l’aigua.
Circuit equivalent
Cada cel·la o vas d’una bateria de plom àcid té com a característica principal la capacitat de mantenir una diferència de potencial elèctric nominal de 2 V (variable en un cert rang en funció del seu estat de càrrega, 1,85 a 2,40 V).
La bateria és, doncs, un generador de voltatge, a diferència de la cèl·lula solar, que ho és d’intensitat. Les bateries reals es diferencien de les ideals o teòriques, en el fet que porten associada una resistència interna en sèrie amb el generador de voltatge, tal com es pot apreciar en la figura.
Aquesta resistència interna,provoca caigudes de tensió segons la llei d’Ohm quan és travessada pel corrent, tant en el procés de càrrega com de descàrrega.
La resistència interna d’una bateria és molt petita, al voltant dels 5 mΩ.
De manera que podem definir el voltatge de la bateria (VB) en funció de l’estat en què es trobi de la següent manera:
- Voltatge en repòs (VBI): és el voltatge en el moment en què la bateria no rep càrrega ni tampoc alimenta consums, aleshores VB serà igual al VBI, ja que com que no passa intensitat, no hi ha caiguda de tensió per efecte de la resistència sèrie.
- Voltatge en càrrega: és el voltatge quan la bateria rep corrent dels mòduls solars, aleshores VB és igual al VBI més la caiguda de tensió en la resistència sèrie; per tant, aquest valor sempre serà superior al voltatge de repòs.
- Voltatge en descàrrega: és el voltatge de la bateria quan aquesta alimenta els consums, aleshores VB serà igual a VBI menys la caiguda de tensió en la resistència interna; per tant, sempre serà inferior a la de repòs.
A mesura que anem carregant la bateria, hi ha més concentració d’àcid de sulfúric en l’electròlit i, per tant, augmenta el valor de VBI, mentre que baixa el valor de la resistència interna.
Quan la bateria s’està descarregant, aleshores el procés s’inverteix, cada cop hi ha més sulfat adherit a les plaques de plom i menys àcid dissolt, baixa el valor de VBI, mentre que augmenta la resistència interna al pas del corrent.
Estat de càrrega en funció de la tensió de la bateria
A mesura que una bateria es carrega, augmenta la diferència de potencial de cada cel·la. La variació de tensió típica d’una cel·la pot variar des d’un valor aproximat d’1,9 V a 2,2 V.
Per tant, la manera més senzilla de comprovar l’estat de càrrega d’una bateria és mitjançant la mesura de la tensió en repòs en els seus borns.
La taula relaciona l’estat de càrrega i la tensió en repòs d’una bateria típica de Pb-àcid.
| Estat de càrrega | Bateria de 2 V | Bateria de 12 V | Bateria de 24 V |
|---|---|---|---|
| < 20 % | 1,90 V | 11,6 V | 23,8 V |
| 25 % | 2,0 V | 12,1 V | 24,2 V |
| 50 % | 2,05 V | 12,3 V | 24,5 V |
| 75 % | 2,15 V | 12,8 V | 25,5 V |
| 100 % | 2,25 V | 13 V | 26,0 V |
Límits de treball d'una bateria
La bateria repeteix de manera cíclica el procés de càrrega i de descàrrega, depenent de la presència o absència del sol.
En aquest funcionament normal de la bateria hi ha dos punts límits de treball (figura):
- Sobrecàrrega: si durant el procés de càrrega la bateria arriba al límit de la seva capacitat i se’l segueix injectant corrent, l’aigua de la dissolució es comença a descompondre produint oxigen i hidrogen (procés de gasificació).
- Sobredescàrrega: hi ha un límit en el procés de descàrrega, passat el qual la bateria es deteriora de manera important, limitant la seva vida útil. Aquest valor límit de descàrrega vindrà determinat pel tipus de bateria.
Per això, el procés de càrrega i de descàrrega ha de ser controlat per un dispositiu extern que s’anomena regulador de càrrega. Aquest dispositiu és l’encarregat d’impedir l’entrada d’energia per sobre de la sobrecàrrega permesa i que es consumeixi més energia que la permesa per la sobredescàrrega.
Tecnologia de les bateries utilitzades en les instal·lacions solars
Les bateries utilitzades tradicionalment en les instal·lacions solars fotovoltaiques són les de tipus àcid-plom, formades per uns elèctrodes (plaques) de plom com a material bàsic immersos en una solució d’electròlit (aigua amb àcid sulfúric).
-

- Un bateria VLRA (Valve regulated lead acid) és una bateria d'àcid plom segellada regulada per vàlvula. Poden ser de tipus gel o AGM. Aquestes bateries són estanques i no requereixen manteniment. La seva vida útil és una mica superior als 10 anys.
Actualment, a més a més de les bateries d’àcid-plom d’electròlit líquid, s’utilitzen altres tipus de bateries:
- Bateries VRLA (Valve regulated lead acid). Són bateries d’àcid-plom regulades per vàlvula, que habitualment reben el nom de bateries segellades. A causa de la seva fabricació no requereix ventilació, es poden muntar en qualsevol orientació (excepte cap avall) i no necessiten manteniment. Podem trobar de dos tipus:
- Bateries de tipus gel. En aquest tipus de bateria l’electròlit no es troba en estat líquid, ja que aquest s’ha immobilitzat mitjançant la incorporació d’una silicona.
- Bateries AGM (Absortion glass mat). En aquest cas l’electròlit s’ha immobilitzat fixant l’àcid en fibres de vidre que l’absorbeix, actuant com una esponja.
- Bateries d’ió-liti. Actualment, són de les bateries més utilitzades en les instal·lacions solars d’autoconsum, ja que admeten sobrecàrregues profundes, la seva vida útil és d’uns 15 anys i no requereixen manteniment. En la figura podeu veure un exemple d’aquest tipus de bateries.
Hi ha dos tipus diferents de bateries de liti en funció de la seva tensió: les d’alt voltatge i les de baix voltatge.
Tipologies de bateries
D’entre els acumuladors electroquímics disponibles en el mercat cal destacar dues tipologies:
La tensió nominal de cada cel·la d’una bateria de liti és d’uns 3,16 V. Per aconseguir tensions nominals més grans les cel·les es connecten en sèrie fins a aconseguir la tensió desitjada. Les més habituals són les de tensió nominal de 48 V.
Pes de les bateries
Un desavantatge de les bateries d’àcid-plom és el seu pes. A partir d’una capacitat de 300 Ah aproximadament s’utilitzen bateries tubulars de 2 V, i s’instal·len en sèrie fins a aconseguir la tensió nominal de la instal·lació (12 V, 24 V o 48 V).
- Acumuladors estacionaris tubulars (figura): construïts amb plaques tubulars i reixes amb baix contingut d’antimoni i formats per un únic vas de 2 V. Això permet fabricar bateries de molta capacitat, ja que en la mateixa envoltant només hi ha un vas. Normalment, s’utilitzaran quan les necessitats de capacitat són elevades.
- Acumuladors compactes o tipus monobloc (figura): inclouen en una mateixa envoltant diferents vasos o elements connectats en sèrie. Com que cada bateria està formada per diferents elements la capacitat que es pot aconseguir és limitada, ja que ve condicionada pel pes del conjunt. Podem trobar bateries monobloc de 6 V, 12 V, 24 V i fins i tot 48 V.
Els principals avantatges dels acumuladors tubulars compostos per elements independents són la facilitat de substitució en cas d’avaria, així capacitats més grans. Per la seva banda, les bateries monobloc ocupen molt poc espai, s’instal·len ràpidament i alhora són molt robustes i compactes.
Característiques tècniques de les bateries
Els paràmetres principals que identifiquen les característiques d’una bateria són els següents:
- Tensió nominal.
- Capacitat nominal.
- Profunditat de descàrrega.
- Vida útil.
- Autodescàrrega.
Tensió nominal
La tensió nominal de la bateria és la tensió elèctrica especificada pel fabricant.
La tensió de funcionament d’una bateria no és constant, ja que depèn de l’estat de càrrega, de la temperatura i d’altres factors.
Elements d'una bateria
Una bateria està formada per l’associació en sèrie d’elements, també anomenats vasos o cel·les. Cada element està format per dos elèctrodes, un de positiu (+) i un de negatiu (-). Cada elèctrode està format per diferent material, de manera que immersos en una solució electrolítica, apareix una tensió en els seus borns.
En les instal·lacions solars petites, és a dir, amb requisits de potència baixa, s’utilitzen les bateries compactes de tipus monobloc. Aquesta bateria està constituïda internament per diferents elements, fins a aconseguir la tensió nominal desitjada. En les instal·lacions solars s’utilitzen bateries de 6 V, 12 V i 24 V.
Hi ha bateries de 48 V de tensió nominal i bateries de tensions nominals superiors.
En instal·lacions de gran potència, s’utilitzen elements individuals, que normalment s’instal·len en sèrie fins a aconseguir la tensió nominal necessària. Aquest tipus de bateria també rep el nom de bateria tubular, per la forma que pren. La tensió d’una bateria tubular depèn del tipus, però normalment és de 2 V.
La tensió d’una cel·la d’una bateria, com podeu veure a la figura depèn del tipus de bateria.
La tensió del banc de bateries d’una instal·lació autònoma determina la tensió nominal de la instal·lació.
Exemple de bateria de 12 V
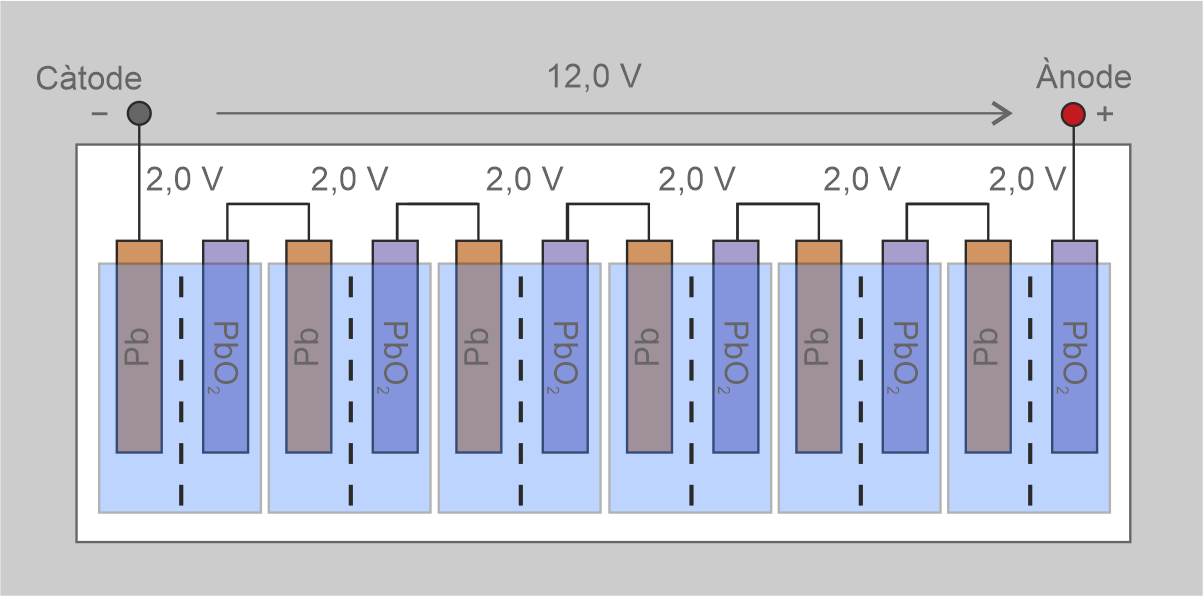
Quan la capacitat necessària és elevada, el pes de les bateries és molt gran, de manera que es comercialitzen bateries tubulars formades per un únic element, generalment de 2 V. Per aconseguir bateries de més tensió es connecten en sèrie fins a aconseguir la tensió desitjada.
En la figura es mostra la connexió de diferents cel·les d’una bateria de Pb-àcid per aconseguir una bateria de 12 V.
Capacitat nominal
El principal paràmetre que defineix una bateria és la seva capacitat nominal.
La capacitat nominal (Ah) és la màxima quantitat d’electricitat que pot emmagatzemar una bateria.
Normalment, la capacitat de la bateria s’expressa en amperes hora (Ah), però depenent de l’aplicació pot indicar-se també en kilowatts hora (kWh):
- Bateries d’instal·lacions d’autoconsum. La capacitat indica la quantitat d’energia que pot emmagatzemar, per tant, la unitat de mesura que s’utilitza és el quilowatt hora (kWh):

- Bateries d’instal·lacions autònomes. En aquest cas la capacitat indica la quantitat de corrent que una bateria pot proporcionar durant un temps determinat. La capacitat de la bateria s’expressa en amperes hora (Ah):
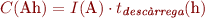
Règim de descàrrega
La quantitat d’electricitat que pot proporcionar un acumulador també depèn del temps de descàrrega, de manera que la capacitat serà més gran com més lentament es produeixi la descàrrega:
Per exemple, si una bateria de 100 Ah es descarrega amb un corrent constant de 5 A, estarà totalment descarregada en 20 hores.


-

- Bateries compacta de tipus gel de tensió nominal 12 V i una capacitat nominal de 100 Ah.
La taula mostra la capacitat de diferents bateries en funció del règim de descàrrega. Valors associats a C10, C20 i C100 representen els temps de descàrrega sobre el qual s’ha establert la capacitat de la bateria (C10 = descàrrega en 10 hores).
| Temps de descàrrega | 10 h | 20 h | 100 h |
|---|---|---|---|
| Capacitat | C10 (Ah) | C20 (Ah) | C100 (Ah) |
| SB 12 / 60 | 52 | 56 | 60 |
| SB 12 / 75 | 66 | 70 | 75 |
| SB 12 / 100 | 88 | 90 | 100 |
| SB 12 / 130 | 105 | 116 | 130 |
| SB 12 / 185 | 155 | 160 | 185 |
| SB 12 / 200 | 162 | 180 | 200 |
| SB 12 / 330 | 260 | 280 | 330 |
Exemple de descàrrega d'una bateria
La capacitat de la bateria SB 12/185 depèn del règim de descàrrega. Per a cada règim de descàrrega, el corrent de descàrrega és diferent:
- Descàrrega en 10 hores: C10 = 155 Ah

- Descàrrega en 20 hores: C20 = 160 Ah

- Descàrrega en 100 hores: C100 = 185 Ah

La figura mostra l’exemple de descàrrega d’un bateria de capacitat nominal de C100 de 185 Ah que alimenta una càrrega de 22 W. La tensió nominal de la bateria és de 12 V.
La tensió del circuit (V) és de 12 V i la potència (P) que se subministra és de 22 W. Per tant, el corrent (I) que subministra la bateria és d’aproximadament 1,83 A:
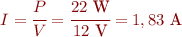
El temps que tardarà a descarregar-se completament la bateria és d’aproximadament 101 hores:
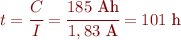
Profunditat de descàrrega
En la pràctica, i per a evitar danys irreversibles a la bateria, tan sols es pot proporcionar una part de la capacitat total, que anomenem capacitat útil. La capacitat útil depèn del tipus d’acumulador i de les condicions de treball, però sol tenir valors des del 40% fins al 80% de la capacitat màxima.
La profunditat de descàrrega és el tant per cent sobre la capacitat màxima de l’acumulador que es pot extreure de la bateria en condicions normals. És un terme molt variable que depèn molt del tipus d’acumulador i que influeix en la seva vida útil.
En les bateries de tipus ió-liti, la capacitat útil és pràcticament del 100%.
La relació entre la capacitat nominal d’una bateria (CNominal) i la seva capacitat útil (CÚtil) depèn de la profunditat de descàrrega (PD):

Estat de càrrega
Durant el funcionament d’una bateria hi ha dos conceptes semblants que ens permeten identificar el nivell de càrrega d’una bateria (vegeu la figura):
- SoC (State of charge): estat de càrrega. Indica com està de plena una bateria.
- DoD (Depth of discharge): profunditat de descàrrega. Indica com està de buida una bateria.
Exemple de capacitat útil d'una bateria
La capacitat nominal (CNominal) d’una bateria és de 185 Ah. La profunditat de descàrrega (PD) que especifica el fabricant és del 80%. La capacitat útil (CÚtil) d’aquesta bateria és de 148 Ah:

Si la instal·lació que utilitza aquesta bateria requereix una capacitat útil de 185 Ah, caldrà utilitzar una bateria de capacitat nominal superior a 231,25 A:

Vida útil
La vida útil d’una bateria se sol mesurar en cicles (més que en anys), de manera que un cicle és un procés complet de càrrega i descàrrega (fins a arribar a la profunditat de descàrrega recomanada).
Les bateries AGM i de tipus gel admeten descarregues més profundes que les bateries de plom àcid obertes. Algunes bateries de liti admeten descàrregues de fins al 100% sense afectar a la seva vida útil.
Si suposem un cicle mitjà d’un cicle per dia i un acumulador ben mantingut, hauria de durar un mínim de 10 anys.
La figura mostra un exemple de les característiques que proporciona un fabricant sobre la vida útil d’una bateria. La capacitat d’una bateria es va reduint a mesura que pateix cicles de càrrega i descàrrega. Com més profunda és la descàrrega, menys cicles suporta la bateria.
La taula mostra la profunditat de descàrrega típica recomanada segons el tipus de bateria:
| Tipus de bateria | Profunditat de descàrrega |
|---|---|
| Pb àcid | 50 % - 60 % |
| VLRA (AGM i Gel) | 70 % - 80 % |
| Liti | 90 % - 100 % |
Autodescàrrega
L’autodescàrrega és un fenomen pel qual un acumulador, per causes diverses, es descarrega lentament però de manera contínua i sense estar connectat a un circuit extern.
La velocitat d’autodescàrrega depèn de diversos factors: temperatura ambient, tipus de bateria…
Com podeu veure a la figura, que mostra un exemple d’especificacions de l’autodescàrrega d’una bateria, a temperatures superiors a 40°C, l’autodescàrrega augmenta considerablement, de manera que passats menys de 4 mesos, una bateria emmagatzemada pot descarregar-se més de la meitat.
Designació de les bateries
La designació d’algunes bateries està formada per la combinació de diverses lletres:
La diferència entre les bateries estacionàries translúcides i transparents, es limita a l’aspecte del recipient, sense afectar les característiques de funcionament.
- O: estacionària.
- P: plaques de plom.
- T: contenidor translúcid.
- C: contenidor opac.
- z: plaques tubulars.
- S: electròlit líquid.
- V: electròlit sòlid, en forma de gel.
Alguns exemples de bateries són les següents:
- OPzS: bateria estacionària d’electròlit líquid amb plaques tubulars.
- OPzV: bateria estacionària de gel amb plaques tubulars.
- TOPzS: bateria estacionària d’electròlit líquid amb plaques tubulars i contenidor translúcid.
La taula mostra la capacitat d’una bateria de tipus OPzV.
La principal diferència entre les bateries OPzS i les OPzV rau en el tipus d’electròlit que utilitzen i el manteniment que requereixen.
La capacitat nominal s’estableix per una tensió final per element d’1,85 V.
| Tipus | Capacitat (Ah) | Tensió nominal | Dimensions (mm × mm × mm ) | Pes (kg) |
|---|---|---|---|---|
| 4 OPzV 240 S | 294 | 2 V | 208 × 105 × 398 | 19,5 |
| 5 OPzV 300 S | 367 | 2 V | 208 × 126 × 398 | 23,5 |
| 6 OPzV 360 S | 440 | 2 V | 208 × 147 × 398 | 28 |
| 5 OPzV 400 S | 519 | 2 V | 208 × 126 × 513 | 32 |
| 6 OPzV 500 S | 623 | 2 V | 208 × 147 × 513 | 36,5 |
| 7 OPzV 600 S | 727 | 2 V | 208 × 168 × 513 | 42 |
| 6 OPzV 720 S | 848 | 2 V | 208 × 47 × 688 | 50 |
| 8 OPzV 960 S | 1.131 | 2 V | 193 × 215 × 688 | 68 |
| 10 OPzV 1200 S | 1.431 | 2 V | 235 × 215 × 688 | 82 |
| 12 OPzV 1400 S | 1.695 | 2 V | 277 × 215 × 688 | 97 |
| 12 OPzV 1700 S | 1.959 | 2 V | 277 × 215 × 838 | 120 |
| 16 OPzV 2300 S | 2.613 | 2 V | 400 × 215 × 815 | 160 |
| 20 OPzV 2900 S | 3.266 | 2 V | 490 × 215 × 815 | 200 |
| 24 OPzV 3500 S | 3.919 | 2 V | 580 × 215 × 815 | 240 |
Les bateries tubulars d’àcid-plom són de 2 V i es poden aconseguir bateries monobloc compactes associant-les en sèrie i paral·lel per obtenir la tensió i capacitat desitjada.
Associació de bateries
Les especificacions dels acumuladors d’una instal·lació vindrà determinada per la capacitat necessària i per la tensió nominal de la instal·lació. Per tant, a vegades caldrà connectar entre si diferents bateries per aconseguir el resultat desitjat.
Associació en sèrie
-

- Exemple de connexió de bateries.
Per aconseguir la tensió necessària sovint utilitzarem la connexió en sèrie de diferents bateries, com la que podeu veure a la figura:
- Com que estan en sèrie, cada bateria (VN) contribueix a la tensió total. La tensió del banc de bateries (VN [banc]) dependrà del nombre de bateries connectades en sèrie (N):

- Com que estan en sèrie i el corrent (I) que subministra cadascuna de les bateries és el mateix, la capacitat total de l’associació és la mateixa que la d’una bateria (CN):

Exemple d'associació en sèrie de bateries
En l’exemple de la figura s’associen 6 bateries de 2 V en sèrie per aconseguir els 12 V nominals d’una instal·lació. La capacitat total no varia (500 Ah):
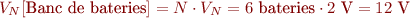

Associació en paral·lel
Sovint no trobem en el mercat bateries amb la capacitat necessària, per tant, s’utilitzarà una connexió en paral·lel com la que podeu veure a la figura:
- Com que estan en paral·lel, la tensió de sortida (VN [banc de bateries]) serà la mateixa que la d’una bateria (VN):
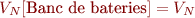
- Com que estan en paral·lel, cada bateria contribuirà al corrent total (I) que subministra i, per tant, la capacitat total de l’associació (CN [banc de bateries]) és la suma de la capacitat de cada bateria(CN). Com que totes les bateries han de ser iguals, la capacitat del banc de bateries dependrà del nombre de bateries instal·lades en paral·lel (M):

Exemple d'associació en paral·lel de bateries
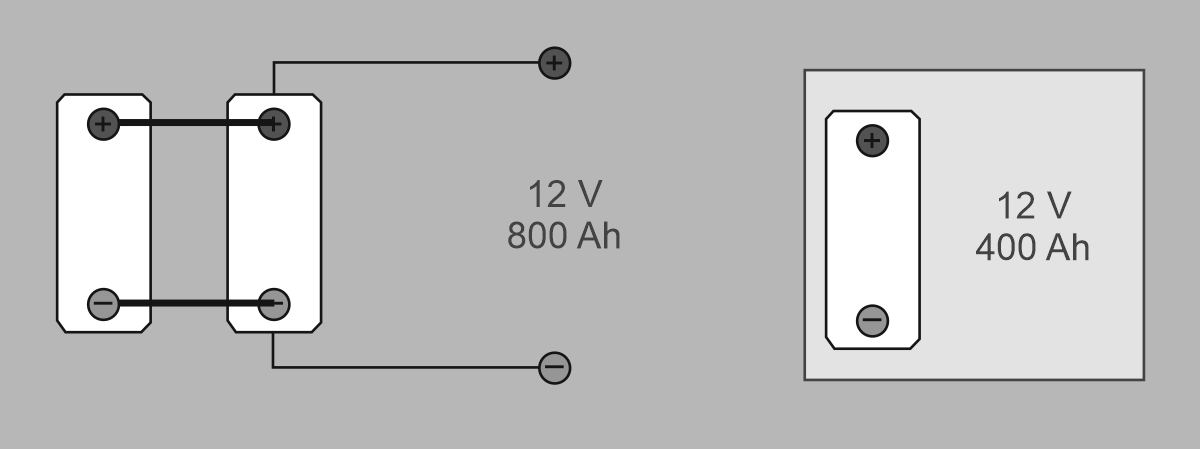
En l’exemple de la figura s’utilitzen bateries compactes de 12 V de capacitat de 400 Ah, però la capacitat que necessitem en una instal·lació és de 800 Ah. Com que no trobem en el mercat bateries d’aquesta capacitat s’opta per connectar dues bateries en paral·lel.
Com que les dues bateries són iguals, la tensió del banc de bateries es manté a 12 V:

La capacitat dels bancs de bateries que resulta de la connexió en paral·lel es duplica, ja que hi ha dues bateries en paral·lel:

Associació mixta
En la connexió mixta de bateries (figura) la tensió de l’associació depèn del nombre de bateries (N) que formen cada branca, mentre que la capacitat total depèn del nombre total de branques (M):


Exemple d'associació mixta de bateries
En l’exemple de la figura s’utilitzen bateries compactes de 6 V de capacitat 200 Ah.
Com que la tensió nominal que es necessita és de 12 V, s’utilitzen branques de dues bateries (N):

La capacitat nominal de cada branca es manté a 200 Ah, ja que estan connectades en sèrie. Quan associen tres d’aquestes branques (M), la capacitat nominal de la connexió es triplica: